Avec le développement continu de la technologie de la biologie moléculaire, la relation entre les mutations génétiques et les défauts et les maladies a acquis une compréhension de plus en plus approfondie.Les acides nucléiques ont attiré beaucoup d'attention en raison de leur grand potentiel d'application dans le diagnostic et le traitement des maladies.Les médicaments à base d'acide nucléique font référence à des fragments d'ADN ou d'ARN synthétisés artificiellement avec des fonctions de traitement des maladies.De tels médicaments peuvent agir directement sur les gènes cibles pathogènes ou les ARNm cibles pathogènes, et jouer un rôle dans le traitement des maladies au niveau du gène.Par rapport aux médicaments traditionnels à petites molécules et aux anticorps, les médicaments à base d'acides nucléiques peuvent réguler l'expression des gènes pathogènes à partir de la racine et ont pour caractéristiques de "traiter les symptômes et de guérir la cause profonde".Les médicaments à base d'acide nucléique présentent également des avantages évidents tels qu'une efficacité élevée, une faible toxicité et une spécificité élevée.Depuis le lancement du premier médicament à base d'acide nucléique, le fomivirsen sodique, en 1998, de nombreux médicaments à base d'acide nucléique ont été approuvés pour le traitement clinique.
Les médicaments à base d'acide nucléique actuellement sur le marché mondial comprennent principalement l'acide nucléique antisens (ASO), le petit ARN interférent (ARNsi) et les aptamères d'acide nucléique.À l'exception des aptamères d'acide nucléique (qui peuvent dépasser 30 nucléotides), les médicaments à base d'acide nucléique sont généralement des oligonucléotides composés de 12 à 30 nucléotides, également appelés médicaments oligonucléotidiques.De plus, les miARN, les ribozymes et les désoxyribozymes ont également montré une grande valeur de développement dans le traitement de diverses maladies.Les médicaments à base d'acide nucléique sont devenus aujourd'hui l'un des domaines les plus prometteurs de la recherche et du développement en biomédecine.
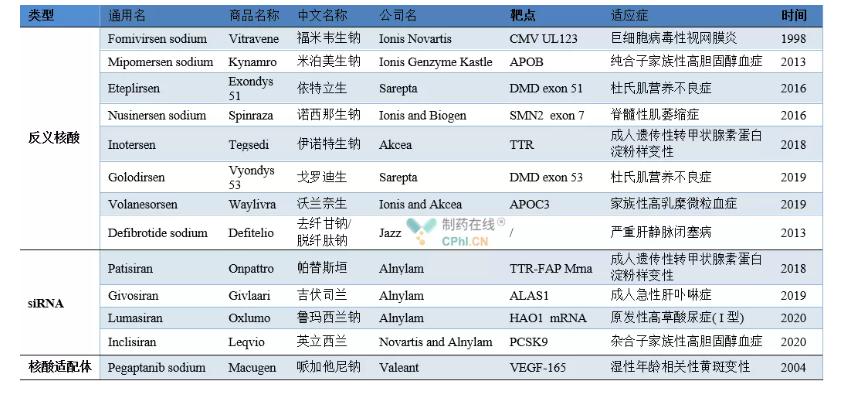
Exemples de médicaments à base d'acide nucléique approuvés
Acide nucléique antisens
La technologie antisens est une nouvelle technologie de développement de médicaments basée sur le principe de la complémentation des bases de Watson-Crick, utilisant des fragments d'ADN ou d'ARN complémentaires spécifiques synthétisés artificiellement ou synthétisés par l'organisme pour réguler spécifiquement l'expression de gènes cibles.L'acide nucléique antisens possède une séquence de bases complémentaire de l'ARN cible et peut se lier spécifiquement à celui-ci.Les acides nucléiques antisens comprennent généralement l'ADN antisens, l'ARN antisens et les ribozymes.Parmi eux, en raison des caractéristiques de stabilité élevée et de faible coût de l'ADN antisens, l'ADN antisens occupe une position dominante dans la recherche et l'application actuelles des médicaments à base d'acide nucléique antisens.
Le fomivirsen sodique (nom commercial Vitravene) a été développé par Ionis Novartis.En août 1998, la FDA l'a approuvé pour le traitement de la rétinite à cytomégalovirus chez les patients immunodéprimés (principalement des patients atteints du SIDA), devenant ainsi le premier médicament à base d'acide nucléique à être commercialisé.Le fomivirsen inhibe l'expression protéique partielle du CMV en se liant à un ARNm spécifique (IE2), régulant ainsi l'expression des gènes viraux pour obtenir des effets thérapeutiques.Cependant, en raison de l'émergence d'une thérapie antirétrovirale à haute efficacité, qui a considérablement réduit le nombre de patients, en 2002 et 2006, Novartis a annulé l'autorisation de mise sur le marché des médicaments Fomivirsen en Europe et aux États-Unis respectivement, et le produit a été suspendu du marché.
Le mipomersen sodique (nom commercial Kynamro) est un médicament ASO développé par la société française Genzyme.En janvier 2013, la FDA l'a approuvé pour le traitement de l'hypercholestérolémie familiale homozygote.Mipomersen inhibe l'expression de la protéine ApoB-100 (apolipoprotéine) en se liant à l'ARNm de l'ApoB-100, réduisant ainsi de manière significative le cholestérol humain des lipoprotéines de basse densité, les lipoprotéines de basse densité et d'autres indicateurs, mais en raison d'effets secondaires tels que la toxicité hépatique, 13 décembre 2012 Le même jour, l'EMA a également rejeté la demande de licence de vente du médicament.
En septembre 2016, Eteplirsen (nom commercial Exon 51) développé par Sarepta pour le traitement de la dystrophie musculaire de Duchenne (DMD) a été approuvé par la FDA.Les patients DMD ne peuvent normalement pas exprimer la protéine anti-atrophique fonctionnelle en raison de mutations du gène DMD dans le corps.Eteplirsen se lie spécifiquement à l'exon 51 de l'ARN pré-messager (pré-ARNm) de la protéine, supprime l'exon 51 et restaure certains gènes en aval L'expression normale, la transcription et la traduction pour obtenir une partie de la dystrophine, afin d'obtenir l'effet thérapeutique.
Nusinersen est un médicament ASO développé par Spinraza pour le traitement de l'amyotrophie spinale et a été approuvé par la FDA le 23 décembre 2016. En 2018, Inotesen développé par Tegsedi pour le traitement de l'amylose héréditaire à transthyrétine chez l'adulte a été approuvé par la FDA.En 2019, Golodirsen, développé par Sarepta pour le traitement de la myopathie de Duchenne, a été approuvé par la FDA.Il a le même mécanisme d'action que Eteplirsen, et son site d'action devient l'exon 53. La même année, Volanesorsen, développé conjointement par Ionisand Akcea pour le traitement de l'hyperchylomicronémie familiale, a été approuvé par l'Agence européenne des médicaments (EMA).Volanesorsen régule le métabolisme des triglycérides en inhibant la production d'apolipoprotéine C-Ⅲ, mais il a également pour effet secondaire d'abaisser le taux de plaquettes.
Le défibrotide est un mélange d'oligonucléotides aux propriétés de plasmine développé par Jazz.Il contient 90% d'ADN simple brin et 10% d'ADN double brin.Il a été approuvé par l'EMA en 2013 et par la suite approuvé par la FDA pour le traitement des veines hépatiques sévères.Maladie occlusive.Le défibrotide peut augmenter l'activité de la plasmine, augmenter l'activateur du plasminogène, favoriser la régulation à la hausse de la thrombomoduline et réduire l'expression du facteur von Willebrand et des inhibiteurs de l'activateur du plasminogène pour obtenir des effets thérapeutiques
ARNsi
L'ARNsi est un petit fragment d'ARN d'une longueur et d'une séquence spécifiques produit en coupant l'ARN cible.Ces siARN peuvent spécifiquement induire la dégradation de l'ARNm cible et obtenir des effets de silençage génique.Comparé aux médicaments chimiques à petites molécules, l'effet de silençage génique des médicaments à base d'ARNsi a une spécificité et une efficacité élevées.
Le 11 août 2018, le premier médicament siRNA patisiran (nom commercial Onpattro) a été approuvé par la FDA et officiellement lancé.C'est l'une des étapes majeures dans l'histoire du développement de la technologie d'interférence ARN.Patisiran a été développé conjointement par Alnylam et Genzyme, une filiale de Sanofi.C'est un médicament siARN pour le traitement de l'amylose héréditaire médiée par la thyroxine.En 2019, le givosiran (nom commercial Givlaari) a été approuvé par la FDA comme deuxième médicament à base d'ARNsi pour le traitement de la porphyrie hépatique aiguë chez l'adulte.En 2020, Alnylam a développé un médicament primaire de type I pour le traitement des enfants et des adultes.Lumasiran avec une oxalurie élevée a été approuvé par la FDA.En décembre 2020, Inclisiran, développé conjointement par Novartis et Alnylam pour le traitement de l'hypercholestérolémie adulte ou de la dyslipidémie mixte, a été approuvé par l'EMA.
Aptamère
Les aptamères d'acide nucléique sont des oligonucléotides qui peuvent se lier à une variété de molécules cibles telles que de petites molécules organiques, de l'ADN, de l'ARN, des polypeptides ou des protéines avec une affinité et une spécificité élevées.Comparés aux anticorps, les aptamères d'acide nucléique ont les caractéristiques d'une synthèse simple, d'un coût inférieur et d'un large éventail de cibles, et ont un potentiel plus large pour l'application de médicaments dans le diagnostic, le traitement et la prévention des maladies.
Le pegaptanib est le premier aptamère d'acide nucléique développé par Valeant pour le traitement de la dégénérescence maculaire liée à l'âge humide et a été approuvé par la FDA en 2004. Par la suite, il a été approuvé par l'EMA et la PMDA en janvier 2006 et juillet 2008 et mis sur le marché.Le pegaptanib inhibe l'angiogenèse grâce à la combinaison de la structure spatiale et du facteur de croissance endothélial vasculaire pour obtenir des effets thérapeutiques.Depuis lors, il a rencontré la concurrence de médicaments similaires Lucentis, et sa part de marché a beaucoup chuté.
Les médicaments à base d'acide nucléique sont devenus un point chaud sur le marché des médicaments cliniques et des nouveaux médicaments en raison de leur effet curatif remarquable et de leur cycle de développement court.En tant que médicament émergent, il fait face à des défis tout en faisant face à des opportunités.En raison de ses caractéristiques exogènes, la spécificité, la stabilité et la délivrance efficace des acides nucléiques sont devenues les principaux critères pour juger si les oligonucléotides peuvent devenir des médicaments à base d'acide nucléique hautement efficaces.Les effets hors cible ont toujours été un point clé des médicaments à base d'acide nucléique qui ne peuvent être ignorés.Cependant, les médicaments à base d'acide nucléique peuvent affecter l'expression des gènes pathogènes à partir de la racine et peuvent atteindre une spécificité de séquence au niveau de la base unique, qui a pour caractéristiques de "traiter la cause profonde et de traiter les symptômes".Compte tenu de la variabilité de plus en plus de maladies, seul le traitement génétique peut obtenir des résultats permanents.Avec l'amélioration continue, la perfection et le progrès des technologies connexes, les médicaments à base d'acides nucléiques représentés par les acides nucléiques antisens, les ARNsi et les aptamères d'acide nucléique déclencheront sûrement une nouvelle vague dans le traitement des maladies et l'industrie pharmaceutique.
Rréférences :
[1] Liu Shaojin, Feng Xuejiao, Wang Junshu, Xiao Zhengqiang, Cheng Pingsheng.Analyse du marché des médicaments à base d'acide nucléique dans mon pays et contre-mesures[J].Journal chinois de génie biologique, 2021, 41(07): 99-109.
[2] Chen Wenfei, Wu Fuhua, Zhang Zhirong, Sun Xun.Progrès de la recherche en pharmacologie des médicaments à base d'acide nucléique commercialisés[J].Journal chinois des produits pharmaceutiques, 2020, 51(12): 1487-1496.
[3] Wang Jun, Wang Lan, Lu Jiazhen, Huang Zhen.Analyse de l'efficacité et des progrès de la recherche sur les médicaments à base d'acide nucléique commercialisés[J].Journal chinois des nouveaux médicaments, 2019, 28(18): 2217-2224.
À propos de l'auteur : Sha Luo, un chercheur et chercheur en médecine chinoise, travaille actuellement pour une grande société nationale de recherche et développement de médicaments et s'est engagé dans la recherche et le développement de nouveaux médicaments chinois.
Produits connexes:
Heure de publication : 19 novembre 2021